 |
 |
 |
 |
 |
| |
|
|
 |
Più eventi avversi con rosuvastatina? |
 |
 |
Inserito il 27 giugno 2005 da admin. - cardiovascolare - segnala a:    
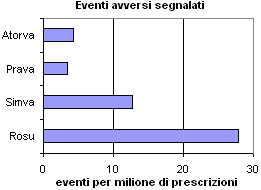 Secondo i risultati di un'analisi postmarketing rosuvastatina sarebbe la statina cui sono associate più frequentemente segnalazioni di reazioni avverse.
Secondo i risultati di un'analisi postmarketing rosuvastatina sarebbe la statina cui sono associate più frequentemente segnalazioni di reazioni avverse.
Le segnalazioni di eventi avversi (ADR) da rosuvastatina raccolte dalla FDA nel primo anno di commercializzazione sono state confrontate con quelle da atorvastatina, simvastatina, e pravastatina nello stesso periodo e nel loro primo anno di commercializzazione; inoltre si sono confrontate anche le ADR da cerivastatina, segnalate nel primo anno di immissione sul mercato. L'endpoint era un indice composito costituto da rabdomiolisi, proteinuria, nefropatia o insufficienza renale. Rosuvastatina, per quasi tutti i confronti operati, è risultata più frequentemente associata in modo significativo (p<0,001) all'endpoint composito. La rabdomiolisi, la proteinuria o l'insufficienza renale tendevano a comparire subito dopo l'inizio della terapia con rosuvastatina (dopo 12 settimane) e con dosi di farmacoanche basse (10 mg o meno). Le ADR da rosuvastatina sono risultate essere più comuni di quelle causate dalle altre statine, nonostante queste abbiano una diffusione molto più ampia, anche per quanto riguarda eventi come tossicità epatica e muscolare senza rabdomiolisi. Questi risultati sostengono i dubbi riguardanti la relativa sicurezza di rosuvastatina alle dosi terapeutiche comunemente impiegate. Le limitazioni dello studio sono quelle legate a tutte le analisi postmarketing delle ADR, tra cui la sottosegnalazione, l'impossibilità di confermare il nesso di causalità o di controllare i fattori di confondimento. Nell'editoriale di accompagnamento, Grundy sottolinea che le problematiche associate alle segnalazioni delle reazioni avverse sono state esaurientemente esaminate nel report di marzo 2005 dell'FDA. In quella sede si concludeva che tutte le evidenze disponibili (inclusi i dati preclinici, gli studi clinici premarketing, gli studi clinici di fase 4 ed i report postmarketing di reazioni avverse) indicavano che rosuvastatina non presentava un rischio di tossicità muscolare superiore a quello delle altre statine e, per quanto riguarda la nefrotossicità, non vi erano dati convincenti. Le segnalazioni di eventi avversi risulterebbero quindi utili per identificare i segnali di tossicità di un farmaco, meno utili invece per una quantificazione del rischio relativo delle diverse molecole appartenenti alla medesima classe. Grundy conclude il suo editoriale proponendo alcuni punti con cui articolare maggiormente il dibattito in atto:
la tossicità di rosuvastatina è di gran lunga inferiore a quella di cerivastatina;
l'incidenza assoluta di miopatia grave associata all'uso di rosuvastatina è molto bassa, comparabile con quella delle altre statine;
in caso si verifichi una miopatia grave, spesso sono presenti fattori di rischio concomitanti per l'insorgenza di questa reazione avversa;
la scelta della statina e della dose terapeutica dovrebbe dipendere da numerosi fattori, tra cui il grado desiderato di diminuzione del colesterolo LDL, i costi e la possibilità di interazioni con altri farmaci;
i medici hanno la responsabilità di conoscere e comprendere il profilo di sicurezza di ciascun medicinale in uso nella pratica clinica affinché la scelta del farmaco e della dose possano bilanciare appropriatamente i benefici ed i rischi legati alla terapia;
le dosi di statine non dovrebbero essere superiori a quelle richieste per il raggiungimento degli obiettivi terapeutici prefissati.
Fonte: Circulation. 2005;111:3051-3057
|
 |
 |
Letto : 1986 | Torna indietro |  | |  | | 
|
 |
 |
 |
 |
|
|
|
© Pillole.org 2004-2026 | Disclaimer | Reg. T. Roma n. 2/06 del 25/01/06 | Dir. resp. D. Zamperini 
ore 22:05 | 116080876 accessi| utenti in linea:
27361
|
| |


