| |
|
|
 |
Rivaroxaban nella prevenzione del tromboembolismo venoso |
 |
 |
Inserito il 03 luglio 2008 da admin. - ortopedia - segnala a:    
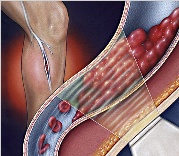 Negli studi RECORD rivaroxaban, un inibitore diretto del fattore Xa, si è dimostrato efficace nel prevenire il tromboembolismo venoso dopo interventi di artroprotesi, con un profilo di sicurezza simile ad enoxaparina
Negli studi RECORD rivaroxaban, un inibitore diretto del fattore Xa, si è dimostrato efficace nel prevenire il tromboembolismo venoso dopo interventi di artroprotesi, con un profilo di sicurezza simile ad enoxaparina
Il rivaroxaban è un inibitore diretto orale del fattore Xa e quindi ostacola la formazione di trombina.
In un primo RCT [1] sono stati reclutati 4541 pazienti sottoposti ad artroprotesi d'anca, randomizzati a rivaroxaban (10 mg una volta al giorno) oppure enoxaparina (40 mg per via sottocutanea una volta al giorno). La durata del trattamento è stata di 31-39 giorni. L'end-point primario era composto da trombosi venosa profonda (sintomatica oppure svelata con venografia), embolia polmonare non fatale, morte da ogni causa a 36 giorni (range da 30 a 42). End-point secondari erano eventi tromboembolici maggiori. L'outcome primario di sicurezza era costituito dai sanguinamenti maggiori. Nell'analisi di superiorità sono stati esclusi 1388 pazienti mentre nell'analisi di sicurezza le esclusioni furono 108. L'end-point primario di verificò in 18 su 1595 pazienti del gruppo rivaroxaban (1,1%) e in 58 di 1558 (3,7%) del gruppo enoxaparina (riduzione assoluta del rischio: 2,6%, IC95% da 1,5% a 3,7%). Sanguinamenti maggiori si verificarono in 6 di 2209 pazienti (0,3%) del gruppo rivaroxaban e in 2 di 2224 pazienti (0,1%) del gruppo enoxaparina ( p = 0,18).
Nel secondo RCT [2] sono stati arruolati 2531 pazienti sottoposti ad artroprotesi di ginocchio. Anche in questo caso, dopo randomizzazione, i pazienti sono stati trattati con rivaroxaban oppure enoxaparina.
La durata del trattamento è stata di 10-14 giorni. L'end-point primario era composto da ogni trombosi venoso profonda, embolia polmonare non fatale o morte da ogni causa entro 13-17 giorni. End-point secondari comprendevano le tromboembolie maggiori e quelle sintomatiche. L'outcome primario di sicurezza era costituito dai sanguinamenti maggiori. L'end-point primario si verificò in 79 di 824 pazienti (9,6%) del gruppo rivaroxaban e in 166 di 878 pazienti (18,9%) del gruppo enoxaparina (riduzione assoluta del rischio 9,2%; IC95% da 5,9 a 12,4). Anche gli eventi tromboembolici maggiori e le trombosi sintomatiche si verificarono in misura minore nel gruppo rivaroxaban. Gli eventi avversi, soprattutto di tipo gastrointestinale, furono il 12% nel gruppo rivaroxaban e il 13% nel gruppo enoxaparina.
Fonte:
1. Eriksson BI et al. for the RECORD1 Study Group. Rivaroxaban versus Enoxaparin for Thromboprophylaxis after Hip Arthroplasty. N Engl J Med 2008 jun 26; 358.2765-2775
2. Lassen MR et al for the RECORD3 Investigators. Rivaroxaban versus Enoxaparin for Thromboprophylaxis after Total Knee Arthroplasty. N Engl J Med 2008 Jun 26; 358:2776-86.
Commento di Renato Rossi
Nei studi studi RECORD 1 e 3 (Regulation of Coagulation in Orthopedic Surgery to Prevent Deep Venous Thrombosis and Pulmonary Embolism) il rivaroxaban, un potente inibitore del fattore Xa somministrabile per os alla dose fissa di 10 mg/die, si è dimostrato superiore alla terapia di controllo (enoxaparina) per quanto riguarda la prevenzione del tromboembolismo venoso dopo interventi ortopedici di artroprotesi, mentre il profilo di sicurezza appare simile. I dati sembrano quindi molto promettenti e il nuovo farmaco è particolarmente attraente perchè può essere somministrato per via orale.
Il programma di studi denominato RECORD comprende in realtà quattro studi, per un totale di oltre 12.500 pazienti. Lo scopo principale di questo programma è stato quello di confrontare il rivaroxaban all'enoxaparina in pazienti sottoposti ad artroprotesi d'anca o di ginocchio. Nello studio RECORD 2 [1] sono stati reclutati 2509 pazienti sottoposti ad artroprotesi d'anca e trattati con enoxaparina (40 mg/die per 10-14 giorni) oppure con rivaroxaban (10 mg/die per 31-39 giorni). L'end-point primario si verificò nel 2% del gruppo rivaroxaban e nel 9,3% del gruppo controllo (riduzione assoluta del rischio 7,3%; p < 0,0001). L'incidenza di sanguinamenti fu la stessa nei due gruppi.
A Nizza [2] al meeting annuale dell'EFORT (European Federation of National Associations of Orthopaedics & Traumatology) sono stati presentati anche i risultati del RECORD 4, in cui 3148 pazienti sottoposti ad artroprotesi di ginocchio sono stati trattati con rivaroxaban (10 mg/die) oppure enoxaparina (30 mg x2/die). La durata del trattamento è stata di 10-14 giorni. L'end-point primario (composto, come negli altri studi gemelli, da tutte le trombosi venose profonde, le embolie polmonari non fatali e i decessi) si verificò rispettivamente nel 6,9% e nel 10,1% (P = 0,012). Il principale end-point di sicurezza (le emorragie maggiori) si verificò nello 0,7% del gruppo rivaroxaban e nello 0,3% del gruppo enoxaparina (differenza non significativa). Non c'erano differenze neppure per quanto riguarda la tossicità epatica. Nello studio RECORD 4 è stata scelta la dose di 30 mg due volte al giorno di enoxaparina perchè negli USA è questa la modalità più usata per la profilassi dopo interventi di artroprotesi.
Interessante è valutare i singoli sotto-end-point dell'outcome primario, perchè si potrebbe essere verificato che la significatività statistica è stata ottenuta solo per una riduzione del tromboembolismo venoso diagnosticato tramite venografia (non che si voglia con questo sminuire l'importanza di questo risultato perchè anche un evento trombotico clinicamente muto potrebbe complicarsi con un' embolia polmonare o, nel futuro, con una sindrome post-flebitica). In realtà negli studi RECORD 2 e 3 si ebbe pure una riduzione statisticamente significativa del tromboembolismo venoso sintomatico (anche se si può obiettare che nel RECORD 2 la durata del trattamento con enoxaparina è stata notevolmente inferiore a causa del disegno stesso del trial). In questi stessi due RCT vi era anche un trend di riduzione dei decessi totali, pur se non statisticamente significativo. Un fatto che ci pare non debba comunque essere trascurato, al di là degli aspetti puramente matematici, perchè non si può escludere, anche se il condizionale è d'obbligo, che su un maggior numero di pazienti il dato avrebbe potuto essere più consistente.
Se i risultati degli studi RECORD saranno confermati (sia sul versante efficacia che su quello sicurezza) rivaroxaban potrà essere un'ulteriore arma nelle mani del medico per la prevenzione del tromboembolismo venoso. Poichè di solito si consiglia di protrarre la profilassi antitrombotica dopo interventi ortopedici maggiori per circa un mese e comunque finchè il paziente deambula, la possibilità di disporre di un farmaco somministrabile per via orale e che non richiede monitoraggio è un altro punto a favore del rivaroxaban perchè, indubbiamente, se ne avvantaggerebbe la compliance dei pazienti.
Particolarmente interessante, inoltre, sarà valutare se il farmaco è efficace anche in altre condizioni: sono attualmente in corso degli studi per testare il rivaroxaban nella fibrillazione atriale e nelle sindromi coronariche acute.
Riteniamo comunque utile un' ultima annotazione: l'esperienza con lo ximelagatran (un antitrombotico per os che agiva inibendo direttamente la trombina, ritirato per grave tossicità epatica) ci induce ad attendere nuovi studi per poter avere un profilo più esaustivo sulla sicurezza del nuovo farmaco. La sicurezza di un farmaco però spesso non può essere pienamente valutata negli studi clinici e, in questo senso, la sorveglianza post-marketing diventa indispensabile.
Referenze
1. Kakkar AK et al. for the RECORD2 Investigators. Extended duration rivaroxaban versus short-term enoxaparin for the prevention of venous thromboembolism after total hip arthroplasty: a double-blind, randomised controlled trial. Lancet 2008 Jul 5; 372:31-39
2. Turpie A et al. Comparison of rivaroxaban--an oral, direct factor Xa inhibitor--and subcutaneous enoxaparin for thromboprophylaxis after total knee replacement (RECORD4: a phase 3 study). European Federation of National Associations of Orthopaedics and Traumatology.
Meeting annuale 2008 20 maggio-1 giugno. Nizza. Abstract n. F85.
|
 |
 |
Letto : 4267 | Torna indietro |  | |  | | 
|
 |
 |
 |
 |
|
|
|


