| |
|
|
 |
Crollano i target di colesterolo, urge critical appraisal della nota 13 |
 |
 |
Inserito il 01 dicembre 2013 da admin. - cardiovascolare - segnala a:    
Crolla il mito dei livelli target di colesterolo a seguito della pubblicazione delle linee guida ACC/AHA sul management delle displipidemie, urge pertanto una profonda rivisitazione della nota 13.
Sono appena uscite nuove Linee Guida Americane [ACC/AHA Guidelines] sul management delle dislipidemie.
Sugli altri contenuti di questo documento occorre riflettere ulteriormente, tuttavia emerge un messaggio forte e chiaro, sempre condiviso dagli autori del presente articolo: il crollo del mito dei target di colesterolemia LDL.
Si dichiara infatti apertamente nella nuova Linea Guida:
"There is no evidence to support continued use of specific LDL-C and/or non- high-density lipoprotein cholesterol (non-HDL-C) treatment targets".
Ciò induce a formulare alcune considerazioni sulla policy regolatoria della prescrizione dei farmaci ipolipemizzanti attuata da anni in Italia.
La teoria delle soglie abbracciata prima da alcune linee guida americane [ATP III REV 2004] e poi dalle Linee guida europee [ESC/ESA 2011] ed in Italia dall AIFA [AIFA 2011, AIFA 2012, AIFA 2013] rappresenta un esempio paradigmatico di distorsione dei risultati della ricerca biomedica. Si tratta nella fattispecie di una tortura dei dati finalizzata ad indirizzare i risultati nella direzione desiderata dal carnefice . Infatti , come avviene per gli esseri umani, sotto tortura i dati possono confermare o smentire qualsiasi cosa [Mills 1999].
Gli studi più citati a sostegno della teoria delle soglie sono 4 [HPS 2002, IDEAL 2005, TNT 2005, PROVE-IT 2004]. Questi trial sono stati programmati per dare risposta ad un quesito fondamentalmente identico: questa statina a questo dosaggio e somministrata per questa durata sarà superiore al farmaco di controllo nel ridurre il rischio dell end-point considerato dalla studio?
I risultati significativi a favore dell intervento rilevati in questi quattro studi (p<0.05 - tutti organizzati su ipotesi di superiorità ) hanno permesso di dichiarare che la statina é risultata superiore al controllo a quelle dosi, su quei pazienti e per quella durata di trattamento.
Ma gli stessi risultati non consentivano in alcun modo di associare l efficacia del trattamento al livello di colesterolemia LDL raggiunto, ragionamento che costituisce al contrario il caposaldo della teoria delle soglie.
Questa puntualizzazione può, in apparenza, risultare strana, illogica o frutto di disquisizioni puramente accademiche. Potrebbe sembrare infatti legittimo associare il risultato di una terapia ipocolesterolemizzante al livello di colesterolemia LDL raggiunto nel braccio di intervento del trial.
Simile interpretazione costituisce, in realtà, il frutto di un analisi ex post, che il protocollo dello studio non aveva previsto, sulla quale non era stato progettato il trial e su cui il campione non era stato tarato. Infine, cosa più importante, linterpretazione stessa è fatalmente condizionata dal tipo di risultato emerso dalla ricerca. Esiste ampio e consolidato accordo in letteratura sul fatto che le conclusioni prodotte da analisi ex post possano essere gravate da alto rischio di distorsioni. I ragionamenti ex post vengono chiamati infatti dai metodologi fishing expeditions [Mills 1999] perchè , proprio come avviene in una spedizione di pesca, non si può mai sapere ex ante cosa si pescherà ex post.
Se uno studio sulle statine fosse stato organizzato per dimostrare il vantaggio di una determinata soglia di colesterolemia LDL rispetto ad un altra i pazienti avrebbero dovuto essere randomizzati a due soglie distinte, non a due trattamenti distinti.
Infatti solo un disegno organizzato in tal modo avrebbe garantito risultati in grado sicuramente di soddisfare o smentire l ipotesi di superiorità ex ante formulata, vale a dire che un abbattimento spinto della colesterolemia LDL possa produrre vantaggi rispetto ad un abbattimento di colesterolemia meno spinto. I trial citati dalle linee guida che sostengono ladozione delle soglie [ESC/ESA 2011, ATP III 2004] non sono stati organizzati in questo modo (sono stati randomizzati farmaci, non soglie) e soprattutto non erano stati progettati per questo scopo, per cui le conclusioni formulate dai documenti di indirizzo che sostengono l adozione di soglie risultano metodologicamente distorte e, di fatto, inaffidabili.
Attribuire l efficacia delle statine al raggiungimento di un livello predeterminato di colesterolemia costituisce un interpretazione osservazionale di risultati sperimentali [Hayward 2006] e raccomandare questo livello nella pratica clinica quotidiana costituisce unindicazione priva di evidenze sperimentali.
A queste interpretazioni ex post dei risultati della ricerca non può essere infatti attribuita la dignita di vere evidenze e, soprattutto, appare quantomeno temerario utilizzare le stesse interpretazioni come consigli operativi nella pratica professionale. Infatti un risultato osservato in una sperimentazione può essere utilizzato confirmatory use [Moye 2003] solo se ha soddisfatto il quesito per cui e stata organizzata ricerca, vale a dire se ha fornito una risposta all ipotesi formulata ex ante sul risultato atteso per lend-point primario. Tutti i risultati non primari e particolarmente le interpretazioni ex post possono solo servire a sostenere il risultato primario (supportive use) o, se con essi discordanti, a generare ipotesi di lavoro (explorative use) [Moye 2003].
Ma indipendentemente dalle considerazioni di metodo, anche adottando il punto di vista (sbagliato) delle linee guida per un utilizzo esplorativo, conservativo e cauto di queste stesse ipotesi non ci sono prove a sostegno dellipotesi così pervicacemente sostenuta. Infatti anche ad una rapida disamina dell ampia e solida letteratura sull impiego delle statine in pazienti ad alto o altissimo rischio, risulta evidente che l efficacia del farmaco non e affatto correlata con il raggiungimento di una determinata soglia. La tabella 1 (che illustra le principali ricerche condotte sull efficacia delle statine nei pazienti in prevenzione secondaria) costituisce soltanto un esempio.
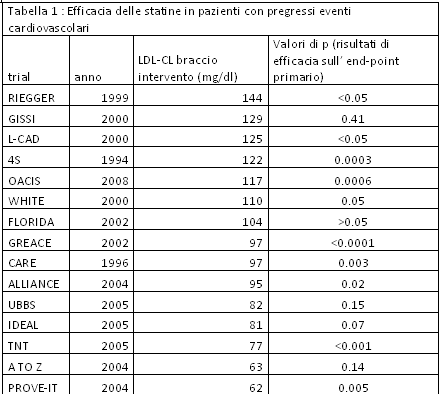
La nota 13 classifica questi pazienti ad altissimo rischio cardiovascolare e li candida al raggiungimento dei valori più bassi di colesterolemia LDL (soglia imposta per questo strato: sotto 70 mg/dl). Solo due studi sui quindici prodotti (tabella I) hanno raggiunto la soglia 70 mg/dl e solo uno di essi ha prodotto risultati significativi.
Anche seguendo la logica dei sostenitori delle soglie risulta insomma assai difficile capire perché in un paziente con coronaropatia debba essere raggiunta per forza una colesterolemia LDL sotto 70 mg/dl quando già nel 1994 lo studio 4s aveva dimostrato che la simvastatina é in grado di ridurre il rischio di end-point fatali e non fatali ad un livello di colesterolemia LDL pari a 122 mg/dl (in altri termini quasi doppio rispetto a quello imposto dalla soglia della nota 13).
Ci sono solide prove che le statine siano efficaci nellallungare l aspettativa di vita e nel ridurre l incidenza di end-point non fatali nei pazienti ad alto od altissimo rischio cardiovascolare (superiore al 20% in dieci anni). Ma che l efficacia dimostrata da queste molecole sia legata esclusivamente allabbassamento del colesterolo LDL non può essere assunto come atto di fede, in quanto questo dogma è facilmente contestabile anche esaminando i semplici dati esposti dalla tabella I.
Se il risultato sugli end-point maggiori dipendesse solo dall abbattimento della colesterolemia LDL , anche trattamenti antiiperlipidemizzanti diversi dalle statine dovrebbero risultare altrettanto efficaci sui pazienti ad alto rischio nell abbassare la mortalità , cosa mai dimostrata con l uso di fibrati. Emerge invece sempre più chiaramente che l efficacia delle statine dipende anche da fattori non strettamente legati alle variazioni della colesterolemia LDL, vale a dire da un insieme di azioni note e non note che complessivamente identificano i cosiddetti effetti pleiotropici di queste molecole. Una recente metanalisi [Bokehold 2012] ha infatti dimostrato che solo il 50% dell efficacia delle statine può essere attribuita alle variazioni di colesterolemia LDL. Ed e importante sottolineare che le metanalisi in cui é stata esplicitamente indagata la natura del rapporto tra abbattimento della colesterolemia LDL e il rischio di eventi cardiovascolari hanno fornito negli ultimi anni risultati ambigui e contrastanti. Secondo alcuni questo rapporto é log-lineare : vale a dire che ad una determinata riduzione di colesterolemia LDL dovrebbe corrispondere una riduzione proporzionale del rischio di eventi [ CTT 2005]; secondo altri la relazione é invece curvilinea : vale a dire che oltre un determinato abbassamento di LDL-CL il vantaggio marginale in termini di rischio risulterebbe irrisorio [Takagi 2013] ; secondo altri il rapporto é imprevedibile perché lefficacia del farmaco non sembra in alcun modo legata al dosaggio del farmaco stesso [Naci 2013]; per altri ancora -addirittura- l associazione potrebbe essere di segno inverso: vale a dire che la mortalità potrebbe aumentare in modo proporzionale all abbassamento di colesterolemia LDL [Razzolini 2008].
La teoria delle soglie non può essere quindi supportata dalla teoria lower is better , che si e sviluppata parallelamente negli stessi anni grazie al contributo di alcuni autori [CTT 2005] : la natura esatta del rapporto matematico-statistico tra variazioni della colesterolemia e rischio eventi cardiovascolari é molto lontana dall essere identificata da un modello preciso. E importante ricordare che le metanalisi del gruppo Cholesterol Treatment Trialists Collaboration [CTT 2005, CTT 2010, CTT 2012] avrebbero potuto fornire preziose informazioni in tal senso perchè costruite sui dataset originali dei singoli trial. Infatti si tratta di metanalisi di dati individuali, dove, attraverso tecniche sofisticate di pooling, vengono elaborati -oltre ai dati aggregati prodotti da ciascun trial, come in qualsiasi metanalisi- anche i dati rilevati a livello dei singoli pazienti. Purtroppo le metanalisi prodotte da questo gruppo di ricerca sono gravate da una serie di problemi di metodo che mettono seriamente in dubbio le conclusioni formulate dai loro autori sulla natura dellassociazione tra colesterolemia LDL ed eventi [Battaggia 2012, Ray 2012, Donzelli 2012, Newman 2012, Mascitelli 2012 ]. Unindicazione sui rapporti esistenti tra interventi, al netto dellazione delle statine, di riduzione della colesterolemia ed eventi potrà venire dallo studio IMPROVE-IT http://clinicaltrials.gov/show/NCT00202878, un ampio RCT i cui risultati sono attesi per il 2014, su pazienti ad alto rischio cardiovascolare, randomizzati a ricevere simvastatina o simvastatina/ezetimibe. In considerazione del meccanismo di azione di ezetimibe, che agisce solo sulla colesterolemia, si potranno avere indicazioni (non prove!) utili in tal senso.
Gli esempi riportati nella tabella I per i pazienti in prevenzione secondaria (che la Nota 13 candida alla soglia 70 mg/dl) sono del tutto estrapolabili alle altre categorie ad altissimo rischio indirizzate dalla nota al raggiungimento di questa soglia.
Per esempio, lo studio SHARP [SHARP 2010] ha reclutato pazienti affetti da insufficienza renale medio-grave (un terzo della casistica era in dialisi): in questi pazienti - solitamente caratterizzati da un alto rischio di morte per infarto e di eventi coronarici - l associazione ezetimibe-simvastatina (scelta evidentemente per la nominale superiore capacità di ridurre la colesterolemia) non ha ridotto la mortalità generale, la mortalità coronarica e lincidenza di infarto.
Ciononostante lassociazione ezetimibe-simvastatina è prevista, come presidio di prima scelta, nellinsufficienza renale e la soglia 70 mg/dl di colesterolemia LDL è stata proposta anche per i pazienti affetti da insufficienza renale grave.
Ancora, in nessuno dei trial in cui le statine erano state sperimentate in soggetti diabetici é stata raggiunta la soglia 70 mg/dl, che viene invece raccomandata nella nota 13 nella maggior parte di questi soggetti (vale a dire nei diabetici sono la maggioranza - in cui la condizione dismetabolica viene accompagnata da almeno un altro fattore di rischio cardiovascolare).
E quindi evidente che le disposizioni regolatorie vigenti incoraggiano il raggiungimento della soglia 70 mg/dl in ampi strati della popolazione generale senza convincenti evidenze scientifiche a supporto di questa scelta.
In base ad una rivisitazione ex post (dati non pubblicati) di dati epidemiologici locali [Bastarolo 2005] questi strati ad altissimo rischio rappresentano circa il 7% della popolazione generale.
Dunque non appare motivato l utilizzo, su larga scala, di farmaci , come l ezetimibe simvastatina, la cui efficacia su end-point non surrogati è stata finora acquisita solo in strati limitati della popolazione e con risultati -a parere di chi scrive- contraddittori (vedi oltre).
L aggiunta di ezetimibe alle statine è in grado di incrementare di circa il 20% la riduzione dei livelli di colesterolemia LDL ottenibili utilizzando le statine da sole [Doggrel 2012] . L associazione è sicuramente in grado, pertanto, di apportare importanti riduzioni dei livelli di LDL-CL ma per gli effetti sugli end-point maggiori sono disponibili due soli trial [SHARP 2010, SEAS 2010] e solo in uno di questi, lo SHARP, sono stati raggiunti - pur con tutti i limiti descritti - risultati clinicamente rilevanti.
Nei pazienti nefropatici, considerati dallo studio SHARP, l associazione ezetimibe-simvastatina ha prodotto una riduzione del rischio di stroke ed una riduzione del numero complessivo di eventi cardiovascolari . La riduzione significativa del numero di eventi cardiovascolari è stata tuttavia conseguita (oltre che dai risultati sullo stroke) grazie ad una riduzione significativa del rischio di rivascolarizzazioni coronariche.
L efficacia del farmaco sulle rivascolarizzazioni coronariche appare in contrasto con la mancanza di efficacia rilevata nello studio SHARP sul rischio di infarto miocardico e sul rischio di morte coronarica, end-point condizionati ovviamente da identica patologia di base . Risulta pertanto difficile accettare la plausibilità biologica dellassunto a fronte di risultati contraddittori.
Non può essere escluso che la riduzione delle rivascolarizzazioni, evidenziata nel trial, rappresenti in realtà un effetto spurio, legato ad un abnorme incremento di rivascolarizzazioni nel braccio assegnato a placebo . In questo caso i benefici prodotti dall ezetimibe in associazione su questo end-point risulterebbero solo apparenti e ciò sarebbe in coerenza con la mancanza di efficacia dimostrata dal farmaco sugli altri end-point vascolari coronarici.
La ragione di un eventuale eccesso di rivascolarizzazioni nel braccio assegnato a placebo potrebbe essere a propria volta associata alla perdita -durante la conduzione dello studio- della doppia cecità garantita al momento della randomizzazione. In confronti statine versus placebo, come lo studio SHARP, il mascheramento dell allocation concealment viene infatti inevitabilmente violato in tempi successivi alla randomizzazione dall abbattimento della colesterolemia che il ricercatore rileva nei primi mesi di trattamento nei pazienti assegnati in cieco alle statine. I ricercatori potrebbero così riporre maggiore attenzione al follow-up clinico dei pazienti assegnati a placebo che, per ansie di natura etica, potrebbero essere sottoposti ad un maggior numero di controlli angiografici . Cio potrebbe ovviamente tradursi in una maggior probabilità di rivascolarizzazioni nel braccio assegnato a placebo rispetto al braccio di intervento (performance bias). Distorsioni di questo tipo nell interpretazione dei risultati sono molto frequenti quando vengono utilizzati nelle sperimentazioni cliniche i cosiddetti end-point physician-driven [Therapeutics 2010, Moye 2003] . Le rivascolarizzazioni coronariche sono appunto outcome physician-driven in quanto non rappresentano un evento naturale ma, piuttosto un evento la cui incidenza viene artificialmente condizionata dalle decisioni dei medici. E dimostrato che l utilizzo di questi end-point (vengono di solito impiegati per aumentare il numero di eventi nel corso della sperimentazione e, di conseguenza, per rendere più efficiente la ricerca tramite riduzione delle dimensioni campionarie) può essere associato ad importanti distorsioni interpretative [Moye 2003] . La letteratura metodologica ha infatti dimostrato che l utilizzo di questi endpoint si associa ad un odds maggiore di significatività statistica (OR 2.24 1.15-4.34) e che gli autori utilizzano spesso questi artifizi per guidare i risultati verso la 'significatività' [Freemantle 2003]. E anche necessario sottolineare che molti dei vantaggi su end-point clinici rilevati da Bajgent & coll. con l uso di statine nei pazienti a basso/medio rischio della metanalisi CTT 2012 [CTT 2012] e nei pazienti nefropatici dello studio SHARP [SHARP 2010] risultano strettamente associati ad una riduzione delle rivascolarizzazioni.
Vista la natura dei risultati clinici prodotti dall ezetimibe-simvastatina nella casistica dello studio SHARP e vista la scarsa trasferibilità di questi stessi risultati a pazienti che non siano nefropatici, appare ancor meno motivata la decisione di estendere l utilizzo dellassociazione a larghi strati della popolazione generale.
Le nuove disposizioni regolatorie della Nota 13 hanno infatti tolto la rosuvastatina (scelta poco comprensibile in base alla logica generale della Nota 13, che valorizza la potenza dei farmaci nell abbassare l LDL colesterolo) dall indicazione, in seconda scelta, nelle ipercolesterolemie ad altissimo rischio cardiovascolare (~7% della popolazione , vedi sopra).
Tenendo conto che ben raramente una statina di prima generazione potrà raggiungere la soglia di LDL-CL indicata per questi soggetti (70 mg/dl) ne consegue che l associazione ezetimibe-simvastatina potrebbe diventare, in teoria, il farmaco più prescritto nello strato di popolazione candidato a questa soglia .
[it]Pertanto le disposizioni regolatorie, per loro natura gravide anche di ripercussioni medico legali, adottate nelle ultime tre versioni della nota 13 appaiono assai discutibili sotto il profilo dell evidenza scientifica [Battaggia 2011, Garattini 2011, Battaggia 2012, Battaggia 2013, Donzelli 2012, Concept paper 2013].[/cit]
La versione 2007 della Nota [Nota 13 2007] aveva indirizzato correttamente la rimborsabilità delle statine ai soggetti caratterizzati da un rischio assoluto di eventi vascolari superiore al 20% a dieci anni. Questa impostazione era in linea con l ampia e consolidata letteratura a sostegno del buon rapporto rischio/efficacia delle statine in questi strati. Queste direttive sono state inoltre seguite da importanti interventi formativi per la diagnosi di Alto Rischio in prevenzione primaria mediante uno score frutto della ricerca italiana e tarato sulla popolazione italiana [Progetto Cuore].
Le nuove versioni della Nota 13 [Nota 13 2011 ,Nota 13 2012 , Nota 13 2013] hanno invece abbracciato punti di vista sostenuti più da illustri opinioni che da evidenze scientifiche, in quanto sostanzialmente si sono avvalse di indicazioni di Linee Guida [ATP 2004, ESC/EAS 2011] considerate dall Istituto Superiore di Sanità di modesta qualità metodologica [Battaggia 2011, Garattini 2011, SNLG-ISS].
Proprio in questi giorni è stato pubblicato un documento firmato dai responsabili European Atherosclerosis Society [EAS Guidelines Committee 2013] a commento delle nuove linee guida americane [ACC/AHA Guidelines]. Gli esperti EAS hanno esplicitamente ammesso in questo documento che i goal terapeutici sulla colesterolemia LDL sono stati fondati su decisioni arbitrarie, ma allo stesso tempo si sono assunti la responsabilità di insistere nel continuare a raccomandarne l uso quale most important tool in daily setting e perché sostenute da a larger pool of knowledge and science in the field [nessuna citazione di queste importanti conoscenze accompagna il documento stesso]. Pertanto per implicita ammissione degli stessi esperti, importanti decisioni strategiche sulla salute cardiovascolare di larghi strati della popolazione mondiale viene affidata più ad opinioni personali che ai contributi della letteratura scientifica.
Negli ultimi anni l utilizzo delle carte del rischio è stato abolito nel 2011, riconfermato nel 2012 e mantenuto nel 2013, ma con abbandono dello strumento italiano a favore di un nuovo strumento (rischio SCORE [Conroy 2003]) messo a punto prevalentemente su popolazioni non italiane.
Nel 2011 sono state quindi introdotte le soglie di colesterolemia LDL, che sono state confermate dalla versione 2012 e che sono addirittura aumentate (da tre a quattro) nella versione 2013. L utilizzo delle statine e stato esteso dal 2011 in poi anche a strati della popolazione a rischio non elevato, nonostante la letteratura abbia finora dimostrato la mancanza di efficacia delle statine su end-point fatali in questi strati di popolazione.
I sostenitori di questa scelta argomentano che le statine sono risultate efficaci nel ridurre gli eventi non fatali anche nei pazienti a rischio basale non elevato. Questa posizione appare assai discutibile sotto il profilo della plausibilità biologica, perché la prima causa di morte naturale in Italia è rappresentata dalle malattie cardiovascolari e non si comprende perché un farmaco, destinato a ridurre il rischio di infarto e di ictus, non debba ridurre significativamente anche la mortalità generale e quella cardiovascolare. Che un farmaco sia efficace sulla morbilità, ma non sulla mortalità implica infatti attente riflessioni sull esatta natura del rapporto rischio/efficacia della terapia negli strati di popolazione a rischio di base non elevato, anche alla luce di potenziali eventi avversi quali, ad esempio, l effetto diabetogeno dimostrato recentemente per questa classe di farmaci [Sattar 2010].
A fronte di dati così contraddittori l estensione della rimborsabilità delle statine agli strati di rischio medio- moderato della popolazione può pertanto costituire, a parere degli scriventi, un opzione potenzialmente non esente da pericoli.
Dal 2011 al 2013, inoltre, e stato progressivamente enfatizzato nei provvedimenti regolatori il concetto efficacia = potenza, che di fatto ha indirettamente promosso la prescrizione di farmaci efficaci su end-point surrogati (ossia sulla colesterolemia LDL) e di efficacia non dimostrata, o solo parzialmente dimostrata, su end-point maggiori (mortalità generale, mortalità cardiovascolare, morbilità cardiovascolare).
L efficacia della rosuvastatina su end-point maggiori è stata per esempio studiata solo in quattro trial, e sono stati osservati risultati clinici significativi solo nello JUPITER [Ridgker 2008], che ha considerato una casistica selettiva (pazienti con elevati livelli di proteina C, quasi metà dei quali affetti da sindrome metabolica). Il farmaco non ha invece prodotto alcun risultato su casistiche parimenti ad alto rischio basale quali i soggetti nefropatici [AURORA 2009] o i pazienti scompensati [CORONA 2007, GISSI-HF 2008].
Inspiegabilmente, nell ultima versione della nota 13, questo potente agente antiiperlipidemizzante è stato escluso dalla rimborsabilità, come seconda opzione di scelta, nei pazienti ad altissimo rischio, che di fatto (vedi sopra) saranno quindi prevalentemente candidati all impiego di ezetimibe simvastatina (che ha prodotto riduzione del rischio di end-point clinici solo nel già discusso studio SHARP).
Le ultime decisioni regolatorie assunte sui farmaci ipolipemizzanti, presentano quindi molte aree di criticità, già evidenziate [Battaggia 2012, Donzelli 2012, Mascitelli 2012, Newman 2012 , Ray 2012] ; e segnalate ai membri della Commissione Tecnico Scientifica dell AIFA ed alla sua Direzione Generale [Concept paper 2013]. E auspicabile che si dia con sollecitudine una pubblica risposta a tali osservazioni. Theres need of a critical appraisal.
Alessandro Battaggia, Luca Puccetti
BIBLIOGRAFIA
ACC/HAH Prevention Guidelines 2013
http://www.pillole.org/public/aspnuke/newsall.asp?id=5952
ARBITER 6-HALTS.
Taylor AJ et al Extended-release niacin or ezetimibe and carotid intima-media thickness. N
Engl J Med 2009 361:2113-22.
ATP III REV 2004
Third Report of the Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (Adult Treatment Panel III)
ATP III Update 2004: Implications of Recent Clinical Trials for the ATP III Guidelines
http://www.nhlbi.nih.gov/guidelines/cholesterol/
AURORA.
Fellstrom BC, et al, for the AURORA
Study Group. Rosuvastatin and cardiovascular events in patients undergoing hemodialysis. N Engl J Med. 2009;
360:1395407
Bastarolo D et al 2005
Indagine per la valutazione del profilo di rischio cardiovascolare nella popolazione di soggetti assistibili afferenti a MMG nell'area della ASL 20 Verona.
Ital Heart J Suppl 2005; 6(6) 382-387
Battaggia A 2011
La Nota 13 è evidence-based? criticità della nuova Nota AIFA
Dialogo sui farmaci n. 4/2011 PAG 178
Battaggia A 2012
I limiti metodologici della metanalisi CTT 2012
Dialogo sui Farmaci n. 4-2012
Battaggia A 2012
Statins for people at low risk of cardiovascular disease
Corrispondence
Lancet Vol 380 November 24, 2012 p1814
Battaggia A 2013
Errare humanum est, perseverare ..
Infofarma n.2
http://www.ulss20.verona.it/infofarma.html
Boekholdt SM et al. 2012
Association of LDL cholesterol, non-HDL cholesterol, and apolipoprotein B levels with risk of cardiovascular events among patients treated with statins.
JAMA 2012; 307: 130209.
Cholesterol Treatment Trialists (CTT) 2005
Collaboration. Efficacy and safety of cholesterollowering treatment: prospective meta-analysis of data from 90 056 participants in 14 randomised trials of statins.
Lancet 2005; 366: 126778.
Cholesterol Treatment Trialists (CTT) Collaboration. 2010
Efficacy and safety of more intensive lowering of LDL cholesterol: a meta-analysis of data from 170 000 participants in 26 randomised trials.
Lancet 2010; 376: 167081.
Cholesterol Treatment Trialists (CTT) 2012
Collaborators.The eff ects of lowering LDL cholesterol with statin therapy in people at low risk of vascular disease: meta-analysis of individual data from 27 randomised trials. CTT. Lancet 2012; doi:
10.1016/S0140-6736: 60367-5
Concept Paper: per una revisione della nota AIFA 13 2013
Infofarma n.1 2013
http://www.ulss20.verona.it/infofarma.html
Conroy RM et al 2003
Estimation of ten-year risk of fatal cardiovascular disease in Europe: the SCORE project
European Heart Journal (2003) 24, 9871003
CORONA 2007
Kjekshus J, et al, for the CORONA Group.
Rosuvastatin in older patients with systolic heart failure. N
Engl J Med. 2007;357:224861.
Doggrel SA. 2012
The ezetimibe controversy can this be resolved by comparing the clinical trials with simvastatin and ezetimibe alone and together?.
Expert Opin Pharmacother
2012; 13: 1469-80.
Donzelli A 2012
Statins for people at low risk of cardiovascular disease
Corrispondence
Lancet Vol 380 November 24, 2012 p1815
EAS Guidelines Committee 2013
The European Atherosclerosis Society
How do they compare with the EAS/ESC guidelines for the management od dyslipidaemia? Comment by EAS Guidelines Committee
[ http://us5.campaign-archive2.com/?u=5722525cab46445583feb00fd&id=4c6ab389e6&e=384788f943 ]
ESC/EAS 2011
European Association for Cardiovascular Prevention & Rehabilitation ESC/EAS Guidelines for the management of dyslipidaemias: the Task Force for the management of dyslipidaemias of the European Society of Cardiology (ESC) and the European Atherosclerosis Society (EAS)
Eur Heart J. 2011; 32:1769-818.
Freemantle N et al 2003
Composite outcomes in randomized trials - Greater precision but with greater uncertain?
JAMA 2003; 289:2554
Garattini S 2011
Cosè successo con la nota 13? Editoriale
Dialogo sui farmaci n. 4/2011 p 143
GISSI-HF 2008
GISSI-HF Investigators.
Effect of rosuvastatin in patients with chronic heart failure (the GISSI-HF Trial): a
randomised, double blind, placebo-controlled trial.
Lancet 2008; 372:1231-9.
HPS 1999
MRC/BHF Heart Protection Study of cholesterol lowering therapy and of antioxidant vitamin supplementation in a wide range of patients at increased risk of coronary heart disease death early safety and efficacy experience.
European Heart Journal. 1999;20:725-41.
Hayward RA et al 2006
Narrative Review: Lack of Evidence for Recommended Low-Density Lipoprotein Treatment Targets: A Solvable Problem
Ann Intern Med. 2006;145:520-30.
IDEAL 2005
Pedersen TR, et al.
Incremental Decrease in End Points Through Aggressive Lipid Lowering (IDEAL) Study Group. High-dose atorvastatin vs. usual-dose simvastatin for secondary prevention after myocardial infarction. The IDEAL study: a randomized controlled trial.
JAMA 2005; 294: 2437-45.
Mascitelli L 2012
Statins for people at low risk of cardiovascular disease
Corrispondence
Lancet Vol 380 November 24, 2012 p1816
Mills JL 1999
Data Torturing
NEJM 1999 329:1196
Moye LA 2003
Miltiple Analyses in Clinical trials -Fundamentals for Investigators
Springer 2003 ISBN 0-87-00727-X
Naci H et al 2013
Comparative benefits of statins in the primary and secondary prevention of major coronary events and all-cause mortality: a network meta-analysis of placebo-controlled and active-comoarators triales
Eur J Prev Card 2013 20(4) 641-657
Newman D 2012
Statins for people at low risk of cardiovascular disease
Corrispondence
Lancet Vol 380 November 24, 2012 p1814
Nota 13 2007
NOTA AIFA 11 - Gazzetta Ufficiale n. 07 Serie generale
del 10.01.2007
Nota 13 2011
NOTA AIFA 11 - Gazzetta Ufficiale n. 163 Serie generale
del 15.07.2011.
Nota 13 2012
NOTA AIFA 12 - Gazzetta Ufficiale n. 277 Serie generale
del 27.11.2012.
Nota 13 2013
NOTA AIFA 13 - Gazzetta Ufficiale n. 83 Serie generale
Del 09.04.2013.
Progetto Cuore
Epidemiologia e prevenzione delle malattie cerebro e cardiovascolari
http://www.cuore.iss.it/valutazione/carte.asp
PROVE.IT 2004
Cannon C. P. et al for the Pravastatin or Atorvastatin Evaluation and Infection TherapyThrombolysis in Myocardial Infarction 22 Investigators Intensive versus Moderate Lipid Lowering with Statins after Acute Coronary Syndromes
N Engl J Med 2004; 350:1495-504.
Ray KK 2012
Statins for people at low risk of cardiovascular disease
Corrispondence
Lancet Vol 380 November 24, 2012 p1816
Razzolini R et al
Non-Cardiovascular Mortality, Low-Density Lipoprotein Cholesterol and Statins: A Meta-Regression Analysis
Cardiology 2008 109:110-116
Ridker,PM et al. Rosuvastatin to Prevent Vascular
Events in Men and Women with Elevated C-Reactive Protein.
N Engl J Med 2008; 359:2195-207.
Sattar N et al 2010
Statins and risk of incident diabetes: a collaborative meta-analysis of randomised statin trials
Lancet 2010; 375: 73542
SEAS 2010
Holme I et al
Observed and predicted reduction of ischemic cardiovascular events in the Simvastatin and Ezetimibe in Aortic Stenosis trial.
Am J Cardiol. 2010 Jun 15;105(12):1802-8
SHARP Collaborative Group. Study of heart and renal protection
(SHARP): randomized trial to assess the effects of lowering lowdensity lipoprotein cholesterol among 9.438 patients with chronic kidney disease.
Am Heart J 2010; 160: 785-94.
SLNG ISS
Ipercolesterolemia: Punteggi AGREE delle Linee Guida selezionate
http://www.snlg-iss.it/cms/files/Tabella%20AGREE_Ipercolesterolemia.pdf
Takagi H et al 2013
Limit to Benefits of Large Reductionsin Low-Density Lipoprotein CholesterolLevels: Use of Fractional Polynomials
to Assess the Effect of Low-DensityLipoprotein Cholesterol Level Reductionin Metaregression of Large Statin
Randomized Trials
JAMA 2013 173(11):1028
Therapeutics Initiative. 2010
April 2010. www.ti.ubc.ca/letter77 (accesso
del 29.08.2012).
TNT 2005
LaRosa J C et al for the Treating to New Targets (TNT) Investigators Intensive Lipid Lowering with Atorvastatin in Patients with Stable Coronary Disease
N Engl J Med 2005; 352:1425-35.
|
 |
 |
Letto : 3567 | Torna indietro |  | |  | | 
|
 |
 |
 |
 |
|
|
|


