
Glitazoni e riduzione della densità ossea

Categoria : metabolismo
Data : 01 gennaio 2008
Autore : admin
Intestazione :
L'uso dei glitazoni č stato associato con una riduzione della densitŕ minerale ossea: analisi dei dati disponibili.
Testo :
I tiazolidinedioni sono una classe di farmaci ipoglicemizzanti largamente utilizzati nel diabete mellito di tipo II. Appartengono a questa classe, il troglitazone, ritirato dal commercio qualche anno fa a causa dei rischi di epatotossicitŕ, il rosiglitazone ed il pioglitazone, attualmente disponibili anche in Italia.
Tali farmaci agiscono come agonisti del PPAR-gamma (peroxisome proliferator activated receptor-gamma), un fattore di trascrizione nucleare che tramite una rimodulazione genica porta ad una riduzione del glucosio, aumentando la sensibilitŕ all’insulina nei tessuti periferici. Oltre all’effetto antidiabetico, l’attivazione del PPAR-gamma influenza l’allocazione delle cellule della linea staminale mesenchimale (MSC) nel midollo osseo. In particolare il rosiglitazone aumenta la differenziazione delle MSC verso gli adipociti e riduce quella verso gli osteoblasti, mentre č ancora incerto l’effetto sugli osteoclasti (1-4).
Il rosiglitazone, introdotto in Europa a partire dal 2000, viene utilizzato in monoterapia o in associazione a metformina o glimepiride ed č controindicato in pazienti con insufficienza cardiaca. Tale farmaco č stato approvato per la commercializzazione sulla base dei risultati dei trial clinici che mostravano la sua capacitŕ nel ridurre i livelli ematici di glucosio e di emoglobina glicata (end-point surrogati) (5).
I dati sugli animali
Topi knock-out per il gene PPAR-gamma presentano una elevata densitŕ ossea, caratterizzata da una aumentata sintesi di osteoblasti da parte dell’osso (6,7), mentre il trattamento di roditori con agonisti PPAR-gamma induce una perdita di osso caratterizzata da una carente funzione degli osteoblasti (3,7,8).
Studi osservazionali sull’uomo
1. Due studi (9,10), non controllati, su pazienti giapponesi con diabete di tipo 2 trattati con troglitazone (glitazone non piů in commercio) hanno riportato significative riduzioni, dopo un mese, nei markers sia di formazione che di riassorbimento osseo, ma con un ritorno ai valori normali entro un anno.
2. Un’analisi piů recente (11) su un piccolo numero (n=69) di soggetti diabetici che assumevano glitazoni (pioglitazone, troglitazone e rosiglitazone) nell’ambito dell’Health, Aging, and Body Composition observational study, ha riportato, in un periodo di piů di 4 anni, una rapida perdita ossea nelle donne, ma non negli uomini.
3. Agli inizi del 2007 (12), la ditta produttrice del pioglitazone e delle associazioni pioglitazone + metformina e pioglitazone + glimepiride ha inviato una lettera agli operatori sanitari per informarli di quanto segue:
“Attualmente a livello mondiale sono stati esposti oltre 7 milioni di pazienti-anno per pioglitazone e circa 40.000 per pioglitazone + metformina. Č stata effettuata un’analisi dei dati dei trial clinici condotti sul pioglitazone soprattutto focalizzando l’attenzione sulle fratture, confrontando pazienti trattati con pioglitazone con pazienti trattati con placebo o con un altro farmaco. La durata massima del trattamento con pioglitazone era 3.5 anni. Nei gruppi trattati con pioglitazone c’erano oltre 8.100 pazienti, mentre nei gruppi di confronto i pazienti erano piů di 7.400, corrispondenti a poco meno di 12.000 pazienti-anno per gruppo. Non c’era un aumento del rischio di fratture fra gli uomini. Tuttavia, c’erano piů segnalazioni di fratture fra le donne trattate con pioglitazone rispetto al gruppo di confronto. La maggior parte delle fratture osservate nelle donne trattate con pioglitazone era a livello dell’arto superiore distale (avambraccio, mano e polso) o dell’arto inferiore distale (piede, caviglia, perone e tibia). L’incidenza calcolata era di 1.9 fratture su 100 pazienti-anno nel gruppo trattato con pioglitazone e di 1.1 fratture su 100 pazienti-anno nel gruppo di confronto. L’eccesso di rischio osservato di fratture nelle donne č di 0.8 fratture su 100 pazienti-anno” Pioglitazone in donne diabetiche trattate per periodi prolungati: aumentata incidenza di fratture. (FDA marzo 2007) http://www.farmacovigilanza.org/servizi/csm-mca/0704-06.asp.
Trial clinici
1. Lo studio ADOPT (A Diabetes Outcome and Progression Trial) era un trial randomizzato in doppio cieco a gruppi paralleli, condotto su pazienti con diagnosi recente di diabete mellito di tipo 2 la cui progressione č stata seguita per 4-6 anni (13). L’obiettivo principale dello studio era quello di confrontare il controllo glicemico con rosiglitazone rispetto a metformina e gliburide in monoterapia in 4360 pazienti randomizzati, di cui 1849 donne, con un’etŕ media di 57 anni.
In questo studio, un numero significativamente piů elevato di donne trattate con rosiglitazone ha sviluppato fratture rispetto alle donne trattate con metformina o gliburide (9,3% vs 5,1% e 3,5% rispettivamente). La maggior parte di queste fratture era a livello degli arti superiori (omero), mano o piede (tabella).
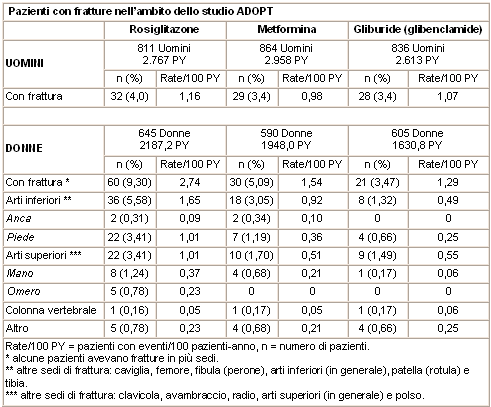
Queste sedi di frattura sono diverse da quelle associate ad osteoporosi post-menopausale (es. anca o colonna vertebrale). L’incidenza osservata di fratture negli uomini era simile nei 3 gruppi di trattamento.
2. Un studio clinico randomizzato (14), controllato con placebo e in doppio cieco č stato recentemente condotto con l’obiettivo primario di determinare se il rosiglitazone induce la formazione ossea (tramite valutazione dei markers ematici P1NP ed osteocalcina) e con l’obiettivo secondario di valutare il riassorbimento osseo (tramite il marker Beta-CTX) e la densitŕ minerale ossea. Lo studio č stato condotto su 50 donne in post-menopausa ed in buona salute, delle quali 25 sono state assegnate per randomizzazione a ricevere rosiglitazone (8 mg/die) e 25 a ricevere placebo, per 14 settimane.
I risultati osservati sono stati i seguenti:
Per i markers osteoblasto-specifici di formazione ossea: riduzione del 13% del P1NP (propeptide N-terminale del procollagene tipo 1) e dell’8% dell’osteocalcina, unitamente ad una riduzione del 17% della fosfatasi alcalina serica.
Per il marker osteoblasto-specifico di riassorbimento osseo: nessuna modifica del Beta-CTX.
Per la mineralometria: riduzione dell’1.9% della densitŕ a livello dell’anca e dell’1.2% a livello delle spine lombari.
Tutti gli effetti osservati erano giŕ evidenti dopo 4 settimane e sono rimasti tali per tutta la durata dello studio.
I risultati di tale studio vanno interpretati anche alla luce del fatto che il diabete di tipo 2 č di per sé un fattore di rischio di fratture negli anziani, sulla base di studi clinici condotti prima che fossero commercializzati i glitazoni (15).
Gli autori (14) di tale trial clinico concludono ad ogni modo che “questo studio dimostra che la terapia a breve termine con rosiglitazone inibisce la formazione ossea ed accelera il riassorbimewnto osseo in donne sane in post-menopausa”.
Le Agenzie Regolatorie
Alcune agenzie regolatorie hanno emesso alcuni comunicati per mettere in guardia gli operatori sanitari sull’aumentato rischio di fratture nelle donne in associazione all’uso dei glitazoni.
Di seguito, si riporta sinteticamente il testo del comunicato lanciato dalla Food and Drug Administration (FDA) (16): da un’analisi dei trial clinici sul pioglitazone č stato osservato un rischio di fratture maggiore nelle donne trattate rispetto al controllo (comparatore attivo o placebo). La maggior parte delle fratture č stata osservata a livello del tratto distale degli arti superiori (avambraccio, mano e polso) o degli arti inferiori (piede, anca, perone e tibia). L’incidenza di fratture č risultata di 1,9/100 pazienti/anno con il farmaco vs 1,1 nel controllo.
Le fratture da glitazoni sono state evidenziate per la prima volta nello studio ADOPT (A Diabetes Outocome Progression Trial) (13) nel dicembre 2006, condotto su 4.360 pazienti, il cui obiettivo era confrontare l’effetto sulla glicemia di rosiglitazone in monoterapia vs metformina o gliburide. In una nota in calce allo studio, veniva segnalato un maggior numero di fratture dell’omero e della mano nei trattati con rosiglitazone.
Inoltre il 7 marzo 2007, anche l’Agenzia Italiana del Farmaco (AIFA) ha pubblicato una Nota Informativa Importante http://www.agenziafarmaco.it/aifa/servlet/wscs_render_attachment_by_id/111.115698.1173796072288.pdf?id=111.115215.1173795021533 sul rosiglitazone in cui viene evidenziato un “aumento dell’incidenza di fratture nelle pazienti di sesso femminile che hanno ricevuto un trattamento a lungo termine”.
Conclusioni
Sebbene siano necessari altri studi per confermare o meno quelli ad oggi esistenti sul rischio di riduzione della massa ossea indotta dai glitazoni, si puň concludere come affermato da Schwartz e Sellmeyer (17) che “i prescrittori dovrebbero essere a conoscenza della possibilitŕ che l’uso dei glitazoni sia associato ad un aumento di demineralizzazione ossea e di rischio di fratture. Contemporaneamente sembra prudente ritenere un paziente a rischio di fratture quando gli viene prescritto un glitazone”.
Fonte: Rosiglitazone e rischio di riduzione di densitŕ ossea: una sintesi delle evidenze. Gianluca Trifirň ed Achille P. Caputi. Dipartimento Clinico e Sperimentale di Medicina e Farmacologia dell’Universitŕ di Messina.
Bibliografia
1. Rzonca SO, et al. Bone is a target for the antidiabetic compound rosiglitazone. Endocrinology 2004; 145: 401-6.
2. Soroceanu MA, et al. Rosiglitazone impacts negatively on bone promoting osteoblast/osteocyte apoptosis. J Endocrinol 2004; 183: 203-16.
3. Ali AA, et al. Rosiglitazone causes bone loss in mice by suppressing osteoblast differentiation and bone formation. Endocrinology 2004; 146: 1226-35
4. Sottile V, et al. Enhanced marrow adipogenesis and bone resorption in estrogen-deprived rats treated with the PPAR-γ agonist BRL49653 (rosiglitazone). Calcif Tissue Int 2004; 75: 329-37.
5. Center for Drug Evaulation and Research. Approval package: Avandia (rosiglitazone maleate) tablets. Company: SmithKline Beecham Pharmaceuticals. Application no. 21-071. Approval date: 5/25/1999. Disponible al sito web: http://www.fda.gov/cder/foi/nda/99/21071_Avandia.htm .
6. Akune T, et al. PPAR-γ insufficiency enhances osteogenesis through osteoblast formation from bone marrow progenitors. J Clin Invest, 2004; 113: 846-55.
7. Pei L, Tontonoz P. Fat’s loss is bone’s gain. J Clin Invest 2004, 113: 805-6.
8. Soroceanu MA, et al. Rosiglitazone impacts negatively on bone by promoting osteoblast/osteocyte apoptosis. J Endocrinol 2004; 183: 203-16.
9. Okazaki R, et al. Short-term treatment with troglitazone decreases bone turnover in patients with type 2 diabetes mellitus. Endocr J 1999; 46: 795-801.
10. Watanabe S, et al. Decrease in serum leptin by troglitazone is associated with preventing bone loss in type 2 diabetic patients. J Bone Miner Metab 2003; 21: 166-71.
11. Schwartz AV, et al. Thiazolidinedione use and bone loss in older diabetic adults. J Endocrinol Metab 2006; 91: 3349-54.
12. http://www.farmacovigilanza.org/goto.asp?page=servizi/csm-mca/0704-06.asp
13. Kahn SE, Haffner SM, Heise MA, Herman WH, Holman RR, Jones NP, Kravitz BG, Lachin JM, O’Neill MC, Zinman B, Viberti G, ADOPT Study Group. Glycemic durability of rosiglitazone, metformin, or glyburide monotherapy.N Engl J Med 2006; 355: 2427-43.
14. Grey A, et al. The peroxisome proliferator-activated receptor-γ agonist rosiglitazone decreases bone formation and bone mineral density in healthy postmenopausal women. A randomized, controlled trial. J Clin Endocrinol Metab 2007; 92: 1305-10.
15. Vestergaard P. Discrepancies in bone mineral density and fracture risk in patients with type 1 and type 2 diabetes- a meta-analysis. Osteoporos Int 2007; 18: 427-44.
16. Short R. Fracture risk is a class effect of glitazones. BMJ 2007; 334: 551.
17.Schwartz AV, Sellmeyer DE. Editorial: thiazolinediones: new evidence of bone loss. J Clin Endocrinol Metab 2007; 92: 1232-4.